日本HTLV-1学会、日本産科婦人科学会、日本産婦人科医会、
日本周産期・新生児医学会、日本新生児成育医学会、日本小児科学会 推奨検査手順
妊産婦診療におけるHTLV-1感染(症)の診断指針
HTLV-1感染の診断指針第1.1版(2018年6月)はこちら![]()
Ⅰ. はじめに
国のHTLV-1母子感染防止対策として2010年11月から妊婦健康診査の項目にHTLV-1抗体検査が公費助成検査項目に追加され、2011年4月には産婦人科診療ガイドランにおいて妊婦に対するHTLV-1抗体検査が推奨レベルA(強く推奨する)に変更となり、多くの妊婦がHTLV-1抗体検査を受けるようになった。
HTLV-1感染(症)の診断はこれまで一次検査と、一次検査陽性者に対する確認検査としてウエスタンブロット(WB)法によるHTLV-1抗体検査が行われてきた。近年、抗体検査法の感度・特異度は向上している一方で、確認検査における「判定保留」が10〜20%を占める点が課題となっている。特に妊婦における「判定保留」の問題は乳汁栄養法の選択にかかわってくるため、正確な感染の有無の判定が望まれてきた。
確認検査における「判定保留」例に対し、末梢血細胞ゲノム中のHTLV-1ウイルスDNA(プロウイルスDNA)を特異的に検出する核酸増幅検査法(genomic PCR法)がHTLV-1感染の確定に有用であることは以前より知られていたが、その標準的な測定方法が確立されていない問題点が残っていた1。この問題に対しては、2014年に厚生労働科学研究班によって標準化が確立され2、2016年4月よりWB法判定保留の妊婦に対してはHTLV-1核酸増幅検査法が保険適用されることとなった。
そこで、日本HTLV-1学会と日本産科婦人科学会、日本産婦人科医会、日本周産期・新生児医学会、日本新生児成育医学会、日本小児科学会は、最新の検査法を利用したHTLV-1感染(症)の正確な診断指針が早期に広く普及するよう、最新の医学知識に則し、HTLV-1核酸増幅検査法を加えた新しい推奨検査手順を「妊産婦診療におけるHTLV-1感染(症)の診断指針」として新たに公表することとした。
Ⅱ. 指針設定の考え方
HTLV-1抗体検査法が進歩した現状を受けて、HTLV-1母子感染予防対策 保健指導マニュアル(2011年3月)3において一次検査の方法として、これまで推奨されてきた抗体検査の粒子凝集(PA)法と化学発光酵素免疫測定(CLEIA)法に加え、化学発光免疫測定(CLIA)法と電気化学発光免疫測定(ECLIA)法が従来の検査法と同等の検査であることが判明したため4-6、CLIA法とECLIA法を追加して推奨する。
また、確認検査で実施するWB法によるHTLV-1抗体検査の判定保留例に対し、HTLV-1核酸増幅検査法によるHTLV-1プロウイルス検出法が一定の有用性を示すとする厚生労働科学研究班の研究結果が得られた2。すなわち抗体を検出するWB法のみでは抗体産生が低い状況でウイルスが存在する場合の確定診断が困難でありHTLV-1 核酸増幅検査法の実施が有効であることが明らかとなった。このような観点から一次検査で陽性となった際、WB法により一次検査の特異性を確認し、その際判定保留になった場合には、HTLV-1 核酸増幅検査法によるHTLV-1プロウイルス検出法にてHTLV-1の感染細胞の検出を行うことにより、より正確で信頼性の高い診断が期待できる。このため確認検査において、判定保留の場合のHTLV-1核酸増幅検査法実施を推奨する。
Ⅲ. 診断法の実際
1. 一次検査
- 当該検査は、妊婦健診を含む妊産婦診療において行われる。
- 診断薬としては、HTLV-1の一次検査法の中から、最新の情報により感度が十分に高い製品を選択することが重要である。
- これまで推奨されているPA法とCLEIA法に加えて、CLIA法とECLIA法を一次検査の推奨検査法とする。
- 一次検査の結果判定とその後の対応は以下の通りとなる。
- A.「陰性」の場合:この時点で「非感染(感染はない)」と判定を確定する。
- B.「陽性」の場合:判定を確定させるため、確認検査を必ず実施する。
2. 確認検査
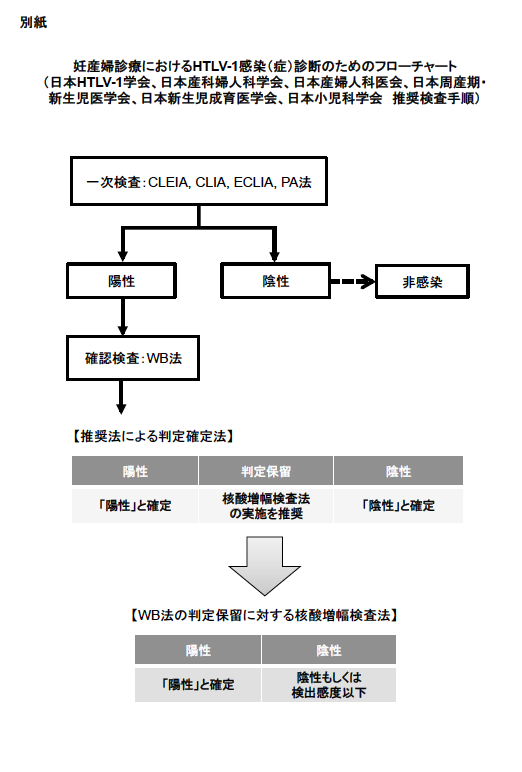
確認検査は、WB法によるHTLV-1抗体検査を実施し、その結果が判定保留の場合にはHTLV-1核酸増幅検査法を実施することを推奨する。診断は、別紙のフローチャートに従う。判定結果は、「陽性」と確定、「陰性」と確定、「陰性もしくは検出感度以下」(4コピー/105細胞未満)のいずれかとなる。
- HTLV-1のWB法が「陽性」の場合:陽性と判定を確定し、HTLV-1感染(症)と診断する。
- HTLV-1のWB法が「陰性」の場合:陰性と判定を確定し、非感染(感染はない)と診断する。
- HTLV-1のWB法が「判定保留」の場合:
- HTLV-1核酸増幅検査法の結果が陽性であれば、陽性と確定する。またHTLV-1感染(症)と診断し、適切な乳汁栄養法(人工乳を原則とするが母乳哺育を強く望む際はエビデンスが十分でないこと、産後の乳房管理が必要であることを説明し、3ヶ月までの短期母乳、凍結解凍母乳)を呈示する。
- HTLV-1核酸増幅検査法の結果が陰性の場合は、陰性もしくは検出感度以下と判定する。検出感度以下の感染の場合は、母子感染の可能性は極めて低いと考えられる7,8(注釈1)。しかしながら、これらの症例に対しての長期母乳の安全性については、結論は未だ出ていない。
注釈1:妊婦末梢血単核球に15コピー/105細胞未満の感染細胞が存在する母親が長期間の授乳をしたとしても、母子感染する可能性は約3%である。従って、本確認検査の検出感度以下(4コピー/105細胞未満)の場合はさらにウイルス量が少ないことから、3%より低くなると考えられる。参考までに、母子感染率3%はHTLV-1感染が確定した母親が、人工乳栄養をした場合の母子感染率とほぼ同程度のリスクである。
[留意事項]
(1) 検査における留意点
- 多くの妊婦は、たとえ一次検査が陽性であっても、確認検査で陽性と確定されない限り「HTLV-1感染(症)」とは診断されないことを知らない。従って医療者は一次検査の陽性者への説明に際しては上記を踏まえたものとしなければならない。すなわち、一次検査の結果が陽性であった場合には、被検者に「一次検査の結果が陽性であり、これから確認検査を行うこと、確認検査の結果が出るまで感染は明らかでないこと」を確実に理解してもらう必要がある。説明を担当する医療者においては、妊婦に「一次検査が陽性=(イコール)感染(症)」との誤解や不安が生じる説明とならないよう配慮し、慎重に対処されたい。
- 本指針はHTLV-1感染(症)の検査時での使用を目的にしたものである。従って、指針中に設定されたHTLV-1核酸増幅検査法は定性的な検査であり、HTLV-1のプロウイルス量の測定(定量検査)を意図したものではない。
- 児で検出される抗体は、母親から児への移行抗体が存在するため、必ずしも児本人の抗体とは限らない。そのため、保護者からの母子感染の診断の希望があった場合、少なくとも出生後3年経ってからのHTLV-1検査を検討する。なお、児への抗体検査は保護者の意思を尊重する。
- HTLV-1核酸増幅検査法では、確認検査での十分な感度を得るためには1 µg程度のgenomic DNAを使用することが望ましい。
(2) 保険診療上の留意点
2016年4月1日HTLV-1核酸増幅検査法はWB法判定保留の妊婦に対してのみ保険適用された。
参考文献
- Kamihira S, Yamano Y, Iwanaga M, et al. Intra- and inter-laboratory variability in human T-cell leukemia virus type-1 proviral load quantification using real-time polymerase chain reaction assays: a multi-center study. Cancer Sci. 2010;101(11):2361-7.
- 厚生労働科学研究費補助金「HTLV-1感染症の診断法の標準化と発症リスクの解明に関する研究」班(代表 浜口功)平成23〜25年度総合研究報告書
- HTLV-1母子感染予防対策 保健指導マニュアル. 厚生労働科学特別研究事業「ヒトT細胞白血病ウイルス-1型(HTLV-1)母子感染予防のための保健指導の標準化に関する研究」班(代表 森内浩幸)平成22年度研究報告書
- Qiu X, Hodges S, Lukaszewska T, et al. Evaluation of a new, fully automated immunoassay for detection of HTLV-I and HTLV-II antibodies. J Med Virol. 2008;80(3):484-93.
- 出口松夫, 鍵田正智, 吉岡範, 他. 6種HTLV抗体測定試薬の基本性能について. 医学と薬学. 2011;66(6):1053-9.
- 園山里美, 宇野直輝, 岡田侑也, 他. HTLV-1/2 抗体測定試薬「エクルーシス試薬Anti-HTLV I/II」の基礎性能評価. 医学検査. 2016;65(6):642-8.
- Li HC, Biggar RJ, Miley WJ, et al. Provirus load in breast milk and risk of mother-to-child transmission of human T lymphotropic virus type I. J Infect Dis. 2004;190(7):1275-8.
- Biggar RJ, Ng J, Kim N, et al. Human leukocyte antigen concordance and the transmission risk via breast-feeding of human T cell lymphotropic virus type I. J Infect Dis. 2006;193(2):277-82.